Desprendimiento prematuro de la placenta normalmente inserta (DPPNI)
Definición
Es la separación de la placenta de su inserción en el útero previa al nacimiento fetal. Normalmente acontece en el tercer trimestre de gestación, aunque puede tener lugar desde el comienzo de la viabilidad fetal, es decir, a partir de la semana 24. Comporta una elevada mortalidad perinatal, así como una alta frecuencia de recidivas en sucesivos embarazos (entre el 5 y el 10%).
Clínica
La tríada clásica es hemorragia, dolor e hipertonía uterina.
A. Sangrado genital (presente en el 80% de los casos). Sangre, generalmente, oscura y no coagulable. También puede aparecer sangre roja y líquido amniótico color vinoso. Puede no guardar relación con la trascendencia de la hemorragia y la extensión del desprendimiento.
B. Dolor abdominal (síntoma menos frecuente que la hemorragia, aparece en un 65% de los casos). Dolor punzante, a modo de lanza que suele ser de aparición brusca y evolución variable. En casos leves suele ser intermitente, dificultando a veces diferenciarlo de la dinámica uterina. En casos más graves el dolor suele ser y aparecer de forma aguda, intensa y brusca desde el comienzo, y suele evolucionar hacia un dolor sordo, localizado en hipogastrio y zona lumbosacra. En muchas ocasiones hay asociación con nauseas, vómitos y sensación de mareo.
C. Hipertonía uterina (aparece en un 50% de los casos). En los casos más graves el útero se pone leñoso y dificulta la auscultación de la frecuencia cardíaca fetal.
D. Hipoxia fetal, según el área de desprendimiento, puede llegar a la muerte fetal.
Diagnóstico
A. Clínico.
El diagnóstico de DPPNI se basa fundamentalmente en la clínica. Se confirma con el examen placentario post-parto.
Exploración.
a. Pérdida de sangre oscura procedente de cavidad uterina.
b. Contracciones uterinas (polisistolia) e hipertonía. Las contracciones cesan a medida que avanza el desprendimiento.
c. Hipotensión materna.
d. Distrés fetal en grado variable.
B. Ecográfico.
La ecografía tiene poca sensibilidad y especificidad en el diagnóstico de DPPNI, habitualmente los signos ecográficos son tardíos. No obstante, descarta otro origen de sangrado importante, como la placenta previa.
La no observación de la zona de desprendimiento placentario no excluye el diagnóstico. También tiene utilidad para el seguimiento de los hematomas retroplacentarios en pacientes con DPPNI asintomáticos en el segundo trimestre e inicios del tercero.
C. Analítico.
Tiene poca trascendencia para la entidad clínica de DPPNI. Sin embrago, el aumento del D-Dímero tiene una especificidad del 93% y un valor predictivo del 91% a la hora de diagnosticar una consecuencia grave, un posible cuadro de CID (coagulación intravascular diseminada).
Complicaciones maternas
A. Anemia.
B. Coagulación vascular diseminada.
C. Shock hipovolémico.
D. Necrosis tubular aguda.
Complicaciones fetales
A. Sufrimiento fetal.
B. Muerte intraútero.
C. IR (La tasa de CIR en casos de DPPNI se multiplica por 2).
Conducta ante la sospecha diagnóstica de DPPNI
La conducta a seguir tiene como base la gravedad del DPPNI. Atendiendo a la clasificación expuesta en el siguiente cuadro, se puede observar que un desprendimiento puede no tener grandes riesgos, complicaciones y evolucionar a un grave estado de compromiso materno-fetal.
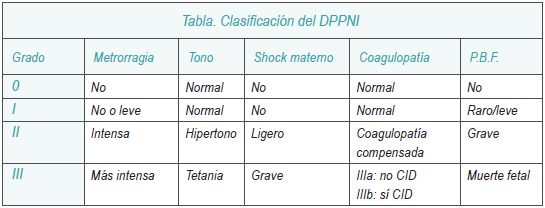
Ante la sospecha diagnóstica de DPPNI, debe procederse del siguiente modo:
Ingreso inmediato de la paciente en sala de partos.
La paciente debe permanecer en vigilancia en sala de partos durante el período de tiempo suficiente para establecer el diagnóstico y descartar la progresión del cuadro de DPPNI.
A. Control de la gestante.
a. Asegurar una vía de perfusión endovenosa. El aporte de fluidos es fundamental en la atención, luego se recomienda tener dos accesos, pudiendo ser unos de ello central con acceso periférico (tipo Drumm). Solución de perfusión: cristaloides, Ringer lactato (más hipotónica).
b. Monitorización de TA, FC, Tª Axilar, inicialmente cada 15 minutos y valorar pérdidas hemáticas.
c. Sondaje vesical y monitorización del flujo urinario. Una diuresis de 50 ml / h asegura una perfusión periférica correcta. Evitar, mediante la sueroterapia, diuresis inferiores a 30 ml / h.
B. Control fetal.
Monitorización cardiotocográfica continua.
C. Analítica urgente.
Hemograma completo.
Ionograma.
Pruebas de función renal: urea, creatinina.
Pruebas de coagulación: T Quick, TTP, fibrinógeno, PDF (D-dímero).
D. Pruebas cruzadas.
Reservar, como mínimo, 4 unidades de sangre total o concentrado de hematíes para prevenir necesidades futuras.
Por cada 4 concentrados de hematíes se debe administrar una unidad de plasma fresco.
E. Ecografía obstétrica.
Intento de localización y medición del hematoma.
Descartar otras causas de sangrado obstétrico.
F. Conducta posterior.
Debe individualizarse en cada caso, se deben evaluar las condiciones obstétricas.
a. Si el desprendimiento es leve, no existe compromiso fetal ni complicaciones maternas (shock, necrosis tubular aguda, necrosis cortical renal o coagulopatía de consumo [-CID-]), y el feto es pretérmino con inmadurez pulmonar, puede intentarse un tratamiento conservador, con monitorización analítica (hemograma completo, pruebas de coagulación, pruebas de función renal y hepática cada 8 horas (durante las primeras 24 horas), y ecográfíca (cada 24 horas). En los casos que asocian amenaza de parto prematuro puede precisarse un tratamiento tocolítico. Se deben administrar, además, aceleradores de la madurez pulmonar fetal.
b. En los casos moderados o severos de DPPNI, ante la aparición de sufrimiento fetal, en gestaciones de > 34 semanas, ante complicaciones maternas o en casos de muerte fetal, debe finalizarse de inmediato la gestación. La vía del parto se individualiza en cada caso, de acuerdo con la edad gestacional, presentación fetal, gravedad del cuadro, condiciones obstétricas y complicaciones maternas. Se recomienda no prolongar el parto más de 5-6 horas.
Independientemente de la vía del parto es preceptiva la práctica de amniotomía. Esta medida permite la colocación de un sistema de registro cardiotocográfico interno y la obtención de microtomas de
sangre fetal. Por otro lado, consigue reducir la presión intraamniótica disminuyendo así, el paso de tromboplastina hística a la circulación y la extravasación de sangre al miometrio.
Complicaciones maternas
A. Coagulación intravascular diseminada (CID).
Una de las causas más frecuentes de CID en obstetricia es el DPPNI.
Aparece como consecuencia del paso de tromboplastina hística a la circulación general desde el hematoma en formación, lo que activa la vía extrínseca de la coagulación. Una coagulopatía con repercusión clínica aparece solo en un 10% de los casos, y es mucho más frecuente en el DPPNI severo (muerte fetal o hemorragia masiva), siendo excepcional en presencia de feto vivo. Antes de la aparición del cuadro analítico que la define (disminución del fibrinógeno, plaquetas < a 50.000 mm3, alargamiento del TTP y disminución del tiempo de Quick), su instauración puede sospecharse por el aumento progresivo de los PDF (productos de degradación del fibrinógeno), que deben ser determinados de forma seriada con una periodicidad aproximada de 4 horas.
El tratamiento se basa en la extracción del feto y la placenta. Después del parto los niveles de fibrinógeno aumentan a razón de 9 mg / 100 ml / hora. La recuperación de la cifra de plaquetas es más lenta, alcanzando valores normales varios días después del parto. La administración de procoagulantes puede ser necesaria si la paciente requiere cirugía y la CID es severa (fibrinógeno < a 50.000 mm3). En estos casos deben suministrarse fibrinógeno y plaquetas. El primero puede administrarse en forma de plasma fresco congelado, (si existe necesidad asociada de expansión del volumen plasmático), o de no ser así, en forma de crioprecipitados. Las plaquetas deben transfundirse si el recuento es inferior a 50.000 mm3. La heparina no está indicada en el tratamiento de la CID asociada a DPPNI a menos que exista evidencia de afectación microvascular (insuficiencia renal progresiva o gangrena digital) y ausencia de sangrado anormal.
B. Necrosis cortical/ Necrosis tubular aguda.
Aparecen como consecuencia del cuadro de Shock. La necrosis cortical aparece precozmente y conduce a la muerte por uremia en una o dos semanas, a menos que se instaure diálisis permanente. La necrosis tubular aguda (NTA) es una complicación más tardía y es reversible en la mayoría de los casos. Ambas entidades pueden prevenirse eficazmente asegurando una buena perfusión tisular mediante la administración de fluidos y la reposición de sangre (mínimo 30 ml / h de diuresis horaria).
C. Hipotensión. Shock.
Surge como consecuencia de la hemorragia. Debe recordarse que en el DPPNI la cuantía de la hemorragia genital no siempre guarda relación con la depleción intravascular, por lo que se tiende a infravalorar la pérdida hemática. En casos de muerte fetal se calcula que la pérdida es superior a los 2,5 l, por lo que se debe trasfundir siempre aunque la paciente esté hemodinámicamente estable. Si no coexisten trastornos de la coagulación, puede ser suficiente la reposición del volumen intravascular mediante la administración de concentrados de hematíes, aunque de preferencia debe administrarse sangre fresca a fin de aportar factores de coagulación. Un buen indicador de la perfusión tisular es el flujo urinario que debe ser como mínimo de 30 ml / h (preferentemente 60 ml / hora).
D. Complicaciones postparto.
En el postparto aumenta el riesgo de hemorragia por atonía y por falta de factores de la coagulación.




